Если молекулы основные структуры В химии задействованы слова, из которых состоят все материалы вокруг нас, а атомы — это буквы, строительные блоки молекул.
Слова бывают разной длины, и типичная молекула также может содержать несколько атомов, несколько сотен или даже сто тысяч атомов.
Молекула поваренной соли NaCl состоит из двух атомов: натрия Na и хлора Cl. Молекула воды H 2 O содержит два атома водорода и один атом кислорода.
Молекула столового сахара C 12 ЧАС 22 О 11 содержит 12 атомов углерода, 11 атомов кислорода и 22 атома водорода, организованных определенным образом.
Откуда мы знаем о существовании атомов? Иногда их можно «увидеть» так же, как мы видим молекулы, которые они могут образовывать.
Не глазами, а более совершенными устройствами.
Один метод использует сканирующий туннельный микроскоп , способный показывать атомы в кристалле или даже перемещать их один за другим.
Другой метод использует нашу способность захватывать ионы (слегка модифицированные атомы — подробности ниже).

На фотографии видно три иона, пойманных одновременно.
На них падает свет, они поглощают его и излучают вновь.
Переизлученный свет можно обнаружить, что позволяет нам увидеть, где находятся ионы, подобно тому, как отражение света от небольшого, но яркого алмаза может помочь нам найти его.
Сколько типов атомов существует? Эти типы называются «химическими элементами», и их точное количество зависит от того, как вы их считаете.
Но давайте предположим, что атомный алфавит состоит примерно из ста химических элементов, а к тонкостям счета мы вернемся позже.
Подобно тому, как мы могли присвоить буквам алфавита от А до Я числа от 1 до 33, так и каждому элементу присваивается не только имя, но и атомный номер (обозначается буквой «Z»).
Простейшие атомы — водород, их атомный номер = 1. Самые сложные в изобилии встречаются в природе, это уран с атомным номером 92. Остальные — кислород (8), азот (7), кальций (20), криптон (36).
), лантан (57), платина (78).
Полный список можно найти на Периодическая таблица элементов Менделеева .
Каждый элемент имеет свой собственный химический состав — то, как он ведет себя внутри молекул — так же, как каждая буква имеет свои собственные правила того, как она может выглядеть в словах.
Вопросы об атомах: 1. Из чего состоят атомы? 2. Что означает атомный номер? 3. Каков основной источник различий в химическом поведении атомов разных элементов? 4. Насколько похожи друг на друга разные атомы одного и того же элемента? 5. Как удерживаются вместе части атома? 6. Почему атомы слипаются и образуют молекулы? Оказывается, на все эти вопросы лучше всего ответить, начав с первого: из чего состоят атомы? Атомы состоят из так называемых «субатомных частиц» (к сожалению, этот термин является неправильным, поскольку эти «частицы» обладают некоторыми свойствами, не присущими частицам).
Точнее, атомы состоят из совокупности маленьких и очень легких электронов, окружающих крошечное, но тяжелое атомное ядро, в котором содержится большая часть массы атома.
Ядро состоит из других «частиц», которые, в свою очередь, тоже состоят из других «частиц», и до них мы доберемся позже.
Ручной атом
Мы часто видим изображения атомов в книгах по химии, рекламе и предупреждающих знаках.Пример — рис.
1. Он дает очень приблизительное представление о том, как работает атом: он имеет определенное количество электронов (синего цвета) снаружи, и они вращаются вокруг центрального атомного ядра.
Ядро представляет собой совокупность протонов (красные) и нейтронов (белые).
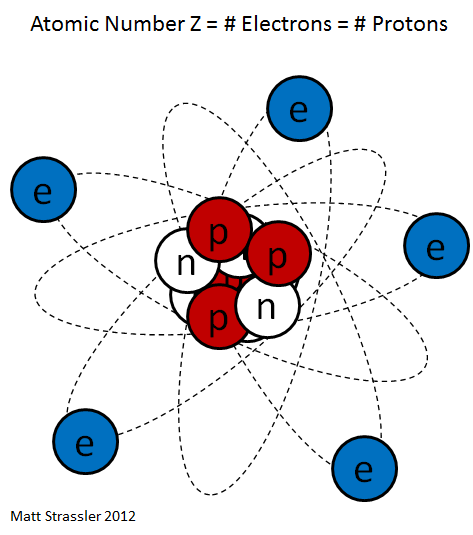
Рис.
1 Теперь мы можем ответить на второй вопрос: что означает атомный номер Z? Это просто количество протонов в ядре.
Кислород имеет атомный номер 8 и имеет в своем ядре 8 протонов.
Проще говоря, атомный номер также равен количеству электронов в атоме.
С количеством нейтронов все сложнее, мы вернемся к этому позже.
Электроны имеют отрицательный электрический заряд (-e), а протоны — положительный электрический заряд (+e).
Нейтроны нейтральны; они не имеют электрического заряда.
Когда число электронов и протонов совпадает, их заряды уравновешивают друг друга, и атом не имеет электрического заряда — такой атом нейтрален.
Но нет ничего необычного – например, в процессе формирования молекул – в том, что атом приобретает или теряет одну или несколько внешних валентность электроны.
При этом электрические заряды электронов и протонов не разрушаются, и образующийся заряженный атом называется ионом.
Более реалистичный атом
Хотя рис.1 примерно описывает архитектуру атома - электроны действительно находятся снаружи, а ядро, состоящее из протонов и нейтронов, посередине - совершенно не передает реальную форму и сущность атома, так как не масштабированы, и мы живем в квантовом мире, в котором объекты ведут себя так, что их трудно нарисовать или представить.
Проблему масштаба можно решить, нарисовав более точное (хотя и несовершенное) изображение, рис.
2. 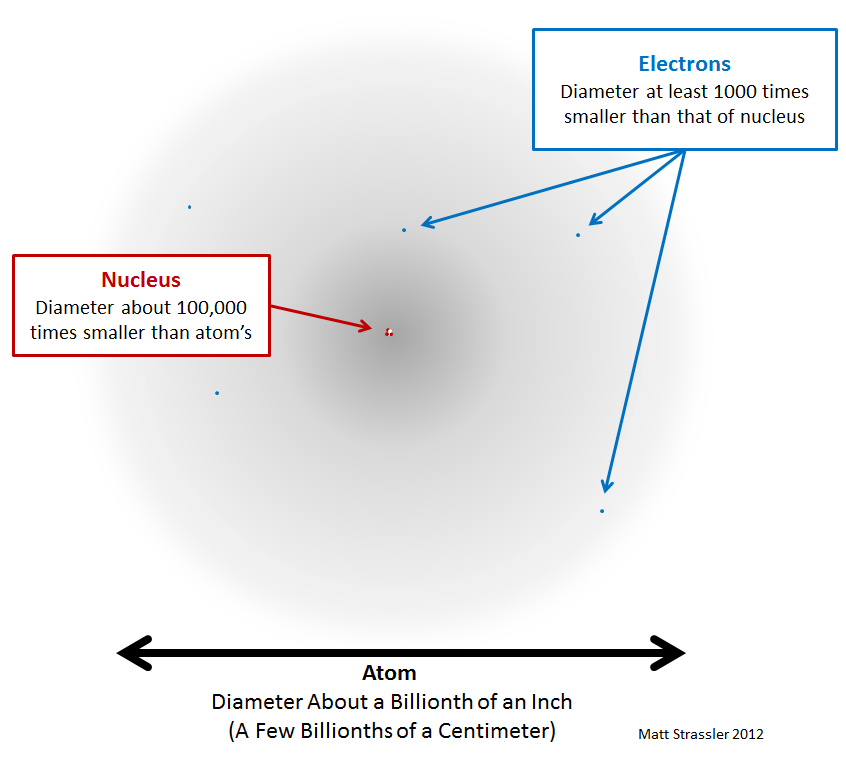
Рис 2. Атом — практически пустой (серая область).
По нему быстро движутся электроны (синие точки, нарисованные не в масштабе, но гораздо большего размера).
В центре — тяжелое ядро (красные и белые точки, нарисованные крупнее масштаба).
Именно это я и пытался передать этим изображением.
Во-первых, электроны очень, очень малы, настолько малы, что мы никогда не могли измерить их размер — они могут быть точечными и не иметь размера, но они определенно не превышают 1/100 000 000 диаметра атома.
Во-вторых, ядра (и протоны с нейтронами, их составные части) тоже чрезвычайно малы, хотя и крупнее электронов.
Их размер был измерен и примерно в 10 000–100 000 раз меньше диаметра атома.
Атом немного похож на деревню.
Протоны и нейтроны в ядре — это большие дома, расположенные в центре деревни, а электроны — это обширные фермерские дома.
На большей части сельской местности растут сельскохозяйственные культуры, а домов нет. И хотя территория, считающаяся частью деревни, может быть и велика, реальная площадь, занимаемая домами, очень мала.
Но эта аналогия не полная, поскольку электроны, в отличие от фермерских домов, очень быстро движутся через серую область на картинке и вокруг ядра со скоростью порядка 1% от скорости света.
Территория, которую они охватывают, обычно не шаровидная, а более сложной формы; кроме того, не все электроны движутся по одной и той же территории.
Но, как я вас предупреждал, рис.
2 тоже не точно.
Во-первых, надо было бы нарисовать ядро в тысячи раз меньше, а электроны — в миллионы раз меньше, только тогда их было бы не видно.
Если бы атом был размером с вашу спальню, его ядро было бы размером с пылинку.
По сравнению со своими компонентами атомы огромны! В каком-то смысле большая часть атома представляет собой пустое пространство! Во-вторых, изображение не передает мрачной природы квантовой механики.
Уравнения квантовой механики описывают и предсказывают поведение молекул, атомов и субатомных частиц, и эти уравнения говорят нам, что эти частицы могут иметь очень странные и неинтуитивные свойства.
Хотя электроны в каком-то смысле точечны (скажем, если бы вы захотели сблизить два электрона, вы бы обнаружили, что можете сдвинуть их вместе на любое расстояние, которое вам нужно, и при этом они не выдадут свою внутреннюю структуру, если она вообще есть), это можно сделать так, что, если оставить их в покое, они разойдутся волной и заполнят все серое пространство на рис.
2. Если это звучит странно, то не потому, что вы чего-то не понимаете: это странно и тяжело об этом думать .
Я, конечно, не знаю, как нарисовать атом, не введя вас в заблуждение, и эксперты до сих пор спорят о том, как лучше всего об этом думать.
Так что пока просто примите это как странный факт. Размер электрона слишком мал, чтобы его можно было измерить, а его масса настолько мала, что электрон может распространиться по всему атому.
Но ядро имеет вполне измеренный и известный размер, а его масса настолько велика — более 99,9% массы всего атома, — что оно вообще не распределено в пространстве.
Ядро находится в середине серой зоны.
Атом и его химия
Лучший способ описать атом, который я могу придумать, состоит в том, что большая часть массы атома содержится в ядре в его центре, вокруг которого распределены чрезвычайно маленькие электроны гораздо меньшей массы, и делают они это совершенно не так, как частицы ведут себя, заполняя всю серую область рис.2. Небольшой размер ядра по сравнению с общим размером атома и тот факт, что оно обычно находится в центре атома, объясняют, почему оно играет относительно слабую роль в химии.
Химия происходит — то есть молекулы образуются и изменяются — когда атомы приближаются друг к другу, и это происходит, когда внешние, валентные электроны одного атома приближаются к внешним электронам другого — когда край серой области одного атома приближается к краю серой области другого.
В химических процессах атомное ядро остается в центрах атомов и никогда не приближается к другим ядрам.
Основная роль ядра — обеспечить положительный заряд, который удерживает электроны, и большую часть массы (которая определяет, насколько трудно другим объектам переместить атом).
Это отвечает на вопрос 3: химия атома в основном определяется деталями, связанными с его внешними электронами.
Эти детали можно узнать (сложным способом, через уравнения квантовой механики) по атомному номеру Z. Вместо изучения химии — темы, которая могла бы занять целый курс — мы спустимся на уровень ниже, к субатомным частицам, попутно отвечая на другие вопросы.
Перечислим проблемы, с которыми мы разобрались, и вопросы, которые еще предстоит изучить.
1. Из чего состоят атомы? Снаружи находятся электроны, в центре — атомное ядро (состоящее из протонов и нейтронов).
2. Что означает атомный номер? Это число протонов в ядре атома, которое в нормальных условиях равно числу окружающих его электронов.
3. Каков основной источник различий в химическом поведении атомов разных элементов? Свойства внешних электронов, определяемые общим количеством электронов каждого элемента, например, атомным номером.
4. Насколько похожи друг на друга разные атомы одного и того же элемента? Об этом мы поговорим в статье об изотопах.
5. Как удерживаются вместе части атома? Мы обсудим это в статье о роли электрических сил и квантовой механики.
6. Почему атомы слипаются и образуют молекулы? Об этом мы поговорим в статье о роли электронов и электрических сил в построении молекул из атомов.
Вот еще один вопрос, который может возникнуть при изучении рис.
2: Если атом по большей части пуст, почему объекты кажутся твердыми? Почему вы не можете дотянуться до экрана компьютера, если экран состоит в основном из пустых атомов? Теги: #Популярная наука #физика #электроны #молекулы #атомы #нейтроны #Мэтт Страсслер #Мэтт Страсслер #Мэтт Страсслер #протоны

-
Гадамер, Ханс Джордж
19 Oct, 24 -
Зельтен, Рейнхард
19 Oct, 24 -
Кофеин
19 Oct, 24 -
Что Такое Бережливый Холст?
19 Oct, 24 -
Конференции Рунета 2014
19 Oct, 24 -
Бизнес-План – Общее Описание Проекта
19 Oct, 24 -
Новый Сайт Маньяко
19 Oct, 24


