В Интернете есть множество инструкций, как сделать «съедобные» батарейки из лимонов и т. д. Но съедобность таких устройств сомнительна, так как электроды, как правило, представляют собой металлические пластины (обычно цинковые и медные), а в Фактически, съедобен только электролит, роль которого играет лимон.
Недавно я задался вопросом, а можно ли создать полностью съедобную батарейку? Сразу поясню, что аккумулятор должен быть сделан не из биосовместимых, а из съедобных компонентов.
Конечно, это можно легко сделать съедобный суперконденсатор из активированного угля, но, как известно, энергоемкость суперконденсаторов очень мала по сравнению с аккумуляторами.
Основная трудность такой идеи – найти подходящие электроды/токосъёмники.
Необходимо, во-первых, чтобы съедобный материал обладал хорошей проводимостью, во-вторых, чтобы он мог участвовать в электрохимических реакциях.
И первое, что приходит на ум, когда думаешь о съедобных проводниках, — это пищевые красители Е174 и Е175, также известные как пищевое золото и серебро.
Но в каких электрохимических реакциях можно использовать эти материалы, если они близки друг к другу в ряду электрохимических напряжений? Но здесь надо помнить, что золото и серебро обладают электрокаталитической активностью.
Где используются катализаторы в электрохимических источниках питания? В топливных элементах! Как работает топливный элемент? Как и другие электрохимические источники энергии, топливные элементы имеют два электрода, погруженных в электролит. Но в отличие от аккумуляторов и суперконденсаторов эти электроды являются не активными материалами, а катализаторами, на которых происходит окисление «топлива», подаваемого извне, и восстановление окислителя.
Например, в классическом примере водородного топливного элемента топливом является водород, а окислителем – кислород. Кстати, по сравнению с другими электрохимическими источниками энергии, например, аккумуляторами и суперконденсаторами, топливные элементы являются наиболее энергоемкими, поскольку работают во время подачи реагентов на электроды.
Но их недостатком является малая мощность, ограниченная скоростью электрохимических реакций и скоростью подачи топлива и окислителя к электродам.

Но вернемся к идее съедобного топливного элемента.
Если кислород воздуха может играть роль окислителя, то что же можно использовать в качестве пищевого топлива? После поиска вариантов топливных элементов в научной литературе я наткнулся на интересное решение.
Оказывается, в качестве топлива можно использовать обычную глюкозу, и этот тип устройств называется абиотический топливный элемент .
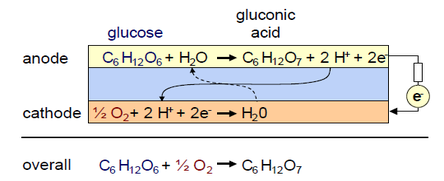
Напряжение таких ячеек обычно не превышает 0,5 В, ток составляет пару десятков микроампер на квадратный сантиметр электрода, поэтому зарядить телефон с помощью такого устройства невозможно, но в настоящий момент для использования разрабатываются абиотические топливные элементы.
в качестве аккумуляторов в биомедицинских микроэлектромеханических системах (БиоМЭМС), которые необходимо имплантировать в организм человека.
Почему «абиотический»? Дело в том, что существует несколько типов топливных элементов, использующих глюкозу в качестве топлива: ферментативные, микробные и абиотические.
«Нзиматические топливные элементы используют изолированные ферменты для окисления глюкозы.
Но проблема в том, что ферменты быстро деактивируются, и такие системы обычно быстро теряют мощность, что является большой проблемой для имплантируемых систем.
В микробных топливных элементах, в свою очередь, используются микроорганизмы, внутреннее применение которых также нецелесообразно из-за риска заражения.
В отличие от описанных выше систем, абиотические топливные элементы используют для переработки глюкозы не живые организмы или биомолекулы, а благородные металлы.
Идеальная конструкция такого устройства такова: два металлических катализатора погружены в раствор глюкозы, содержащий также растворенный кислород. При этом один из электродов является селективным катализатором окисления глюкозы, а другой – восстановления кислорода.
То есть съедобный топливный элемент теоретически можно было бы сделать в виде сладкого желе, покрытого с одной стороны пищевым золотом, которое окисляло бы глюкозу, а с другой — серебром, которое восстанавливало бы кислород. Но будет ли работать такое устройство? И здесь мы сталкиваемся со второй трудностью при создании съедобного топливного элемента: большинство благородных металлов обладают каталитической активностью как при окислении глюкозы, так и при восстановлении кислорода.
То есть, даже если серебро менее «чувствительно» к глюкозе и обладает лучшей каталитической активностью по восстановлению кислорода, напряжение нашей ячейки будет меньше 0,5 В, поскольку реакция восстановления кислорода будет происходить параллельно на аноде и катоде.
В общем, хотелось бы проверить эти теоретические мысли на практике, поэтому в следующих постах речь пойдет о попытках сконструировать съедобный абиотический топливный элемент в домашних условиях.
Теги: #Энергия и аккумуляторы #топливный элемент

-
Гугл 2017
19 Oct, 24 -
Компьютерный Рассказ О Будущем Mac И Пк :)
19 Oct, 24 -
Canon Выпускает Первые Принтеры С Снпч
19 Oct, 24


